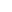Adv Sci:澳门大学邓初夏等团队发现前列腺癌“双重间谍”蛋白GNL3,既驱动增殖又介导免疫逃逸,联合靶向提供治疗新思路
发表时间:2026-03-11雄激素受体(AR)信号是去势抵抗性前列腺癌(CRPC)的主要致癌驱动因素,但其具体机制尚未完全阐明。
2026年3月2日,澳门大学Edwin Cheung、邓初夏共同通讯在Advanced Science(IF=14.1)在线发表题为GNL3 Orchestrates AR Transcriptional Programs to Drive Castration-Resistant Prostate Cancer and Immune Evasion的研究论文。
通过对CRPC细胞和原发性前列腺癌(PCa)细胞进行蛋白质组分析,研究鉴定出核仁G蛋白3(GNL3)是一种新型的AR共调控因子。GNL3可与AR发生物理相互作用,增强其在染色质上的结合,并直接共激活包括NEK2和CDC20在内的、促进细胞增殖的转录程序。
同时,GNL3通过I类组蛋白去乙酰化酶(HDACs),对CXCL10、TAP1等免疫应答基因发挥共抑制作用,进而促进CD8+T细胞清除,并构建免疫抑制型肿瘤微环境。从正常前列腺组织到CRPC,GNL3表达水平及AR-GNL3复合物形成均呈渐进性升高,并与不良临床预后相关。
功能实验表明,敲低GNL3可使CRPC细胞对AR拮抗剂增敏,并抑制肿瘤生长与转移。此外,研究证实联合抑制NEK2、I类HDACs与AR信号可作为CRPC的潜在治疗策略。综上,本研究证实GNL3是一种具有双重功能的AR共调控因子及治疗靶点,为晚期前列腺癌的转录调控与免疫逃逸机制提供了新的理论依据。

前列腺癌(PCa)是全球男性中第二常见的癌症。雄激素受体(AR)信号通路在前列腺癌的发生与进展中发挥关键作用。尽管通过手术或药物去势的雄激素剥夺治疗(ADT)仍是原发性前列腺癌的一线标准治疗方案,并可显著延长患者生存期,但多数患者最终会复发并产生耐药,进展为去势抵抗性前列腺癌(CRPC),这是前列腺癌中侵袭性极强、预后极差的阶段。
即使在雄激素剥夺后,CRPC中AR信号仍常被异常激活,其典型表现为血清前列腺特异性抗原(PSA)水平升高,而PSA是公认的AR下游靶基因与临床诊断标志物。
多种机制参与CRPC中AR的重新激活,这些均可导致AR持续性激活。肿瘤细胞内的雄激素原位合成也是维持CRPC中AR信号持续活化的重要原因。除上述经典机制外,AR共调控网络的异常已成为去势抵抗的关键驱动因素。然而,CRPC中仍有大量AR共调控因子尚未被鉴定,其在CRPC中的作用也知之甚少。
AR介导的转录调控需要多种辅助因子在AR结合位点(ARBS)上协同组装。这些辅助因子主要分为三类。第一类为先锋因子,可通过重塑染色质结构促进AR与特定基因组位点结合。第二类为共调控因子,这类非DNA结合蛋白可精细调控AR的转录活性。第三类为协同因子,可促进AR转录复合物的募集。解析这些辅助因子的组成与功能,对于阐明AR驱动的致癌程序及治疗耐药机制至关重要。
新兴证据表明,免疫学上“冷”的肿瘤微环境(TME)有助于CRPC的进展。PCa通常表现出低T细胞浸润,且对免疫检查点阻断疗法反应较差。更具侵袭性的亚型,其CD8+ T细胞存在甚至低于良性前列腺增生(BPH)和原发性PCa。
近期机制研究表明,AR信号在塑造这一免疫抑制格局中起到了作用。具体来说,AR抑制了T细胞中的干扰素信号和肿瘤细胞中的MHC I类表达,导致PCa免疫逃避和免疫治疗耐药性。
此外,巨噬细胞中的AR激活诱导IL-1β的分泌,推动骨髓系来源抑制细胞(MDSCs)的积累,并抑制CD8+ T细胞活性。虽然靶向致癌通路如PI3K信号或染色质调控因子已显示出重编程TME和增强抗免疫的前景,但AR共调控因子在调节免疫反应中的作用仍大多未被充分探讨。

GNL3通过抑制免疫应答基因CXCL10和TAP1减少CD8+T细胞的浸润与活化(摘自Advanced Science)
本研究通过基于蛋白质组学的内源性蛋白快速免疫沉淀(RIME)技术,在CRPC细胞中鉴定出核仁G蛋白3(GNL3)为新型AR共调控因子。临床样本分析显示,GNL3在前列腺癌中表达上调,并在CRPC中达到峰值,其高表达与患者不良预后相关。结合分子生物学、基因组学、单细胞分析及成像质谱流式(IMC)等技术发现,GNL3与AR协同调控转录程序,在促进细胞增殖的同时抑制免疫应答基因,进而构建免疫抑制性前列腺癌肿瘤微环境。
最后,本研究证实联合抑制NEK2、I类组蛋白去乙酰化酶(HDACs)与AR信号可在体内显著增强抗肿瘤效果,为CRPC提供了极具前景的治疗策略。